Accident de Tchernobyl (Ukraine - 1986)
État des connaissances sur les conséquences sanitaires des accidents nucléaires de Tchernobyl et Fukushima
22/04/2026
Les accidents de Tchernobyl et de Fukushima sont les deux accidents nucléaires majeurs, classés au niveau maximal de l’échelle internationale des événements nucléaires (INES). L’accident de Tchernobyl est survenu le 26 avril 1986 en Ukraine lors de la réalisation d’un essai technique, provoquant l’explosion d’un réacteur et un gigantesque incendie qui ne sera éteint définitivement que treize jours plus tard. L’accident de Fukushima est survenu le 11 mars 2011 au Japon à la suite d’un tremblement de terre et d’un tsunami. Les niveaux de contamination ont été plus faibles autour de la centrale nucléaire de Fukushima Daiichi qu’autour de celle de Tchernobyl.
A la suite de ces deux accidents, de nombreux programmes de recherche et études épidémiologiques ont été et sont menés sur les conséquences sanitaires pour les intervenants et les populations affectées. Cette note d’information en propose une synthèse. Elle traite principalement des risques de cancer de la thyroïde chez les personnes exposées aux rayonnements ionisants pendant l’enfance et l’adolescence, mais aussi des autres types de cancers et effets non cancéreux de l’exposition aux rayonnements ionisants, notamment chez les travailleurs intervenus lors de ces accidents.
1. Les effets sanitaires à court terme
Accident de la centrale de Tchernobyl
Suite à l’accident, environ 530 000 personnes civiles et militaires, appelées « liquidateurs », ont participé à l'intervention d'urgence, au confinement et au nettoyage sur le site de Tchernobyl et dans les zones contaminées après l’accident. Environ 240 000 d’entre elles étaient présentes en 1986 et 1987, au moment où les doses étaient les plus élevées sur le site du réacteur et dans la zone environnante des 30 km. La dose efficace moyenne reçue par les liquidateurs entre 1986 et 1990, principalement due à une irradiation externe, est estimée à environ 120 mSv (UNSCEAR 2000, UNSCEAR 2011), mais certains liquidateurs qui sont intervenus dans les premières semaines ont pu recevoir des doses supérieures à 1 Sv.
Les 600 pompiers et personnels de la centrale qui sont intervenus le premier jour de l’accident ont reçu les doses de rayonnements ionisants les plus élevées : deux d’entre eux sont décédés immédiatement de brûlures et 28 sont décédés des suites de leur irradiation dans les quatre premiers mois qui ont suivi l’accident. Au total, un syndrome aigu d’irradiation (SAI) a été diagnostiqué chez 134 intervenants et pompiers. Parmi les survivants, une dégénérescence cutanée secondaire à des brûlures radiologiques et des cataractes sont les principales séquelles observées aujourd’hui.
Accident de la centrale de Fukushima Daiichi
En termes de conséquences sur la santé des travailleurs, l’accident de la centrale nucléaire de Fukushima Daiichi diffère de celui de Tchernobyl à bien des égards.
Environ 25 000 travailleurs ont été employés entre mars 2011 et octobre 2012 dans des opérations d’urgence et de remédiation sur le site de la centrale nucléaire de Fukushima Daiichi. La dose efficace moyenne de ces travailleurs au cours des 19 premiers mois après l’accident était de l’ordre de 12 mSv, soit 10 fois moins que celle reçue par les liquidateurs de Tchernobyl. À Fukushima, 35 % des travailleurs ont reçu une dose totale de plus de 10 mSv sur cette période et 0,7 % une dose totale de plus de 100 mSv. La dose efficace maximale rapportée est de 679 mSv (UNSCEAR 2014). Aucun syndrome aigu d’irradiation ni décès pouvant être attribué à une exposition aux rayonnements ionisants n’ont été observés parmi les travailleurs engagés dans des travaux d’urgence.
2. Les effets sanitaires à long terme
2.1. Les cancers de la thyroïde après un accident nucléaire
À ce jour, le cancer de la thyroïde chez les personnes exposées pendant l’enfance et l’adolescence est le principal effet sanitaire démontré associé aux retombées radioactives de l’accident de Tchernobyl, dû à l’iode 131.
Après l’accident de la centrale de Fukushima Daiichi, en se basant sur l’expérience acquise lors de l’accident de la centrale de Tchernobyl, un dépistage systématique du cancer de la thyroïde a été mis en place dans la préfecture de Fukushima chez les jeunes âgés de moins de 18 ans au moment de l’accident. À ce stade, environ 15 ans après l’accident, il est encore prématuré de se prononcer sur une éventuelle augmentation des cancers de la thyroïde due à l’accident de Fukushima Daiichi.
2.1.1. Ce qu’il faut savoir sur le cancer de la thyroïde
La thyroïde est une glande située au niveau du cou dont la fonction principale est de fabriquer des hormones à partir de l’iode présent naturellement dans l’alimentation (poissons, fruits de mer, laitages…). Ces hormones thyroïdiennes sont indispensables au bon fonctionnement de l’organisme et, en cas d’ablation de la thyroïde, un traitement hormonal substitutif est prescrit à vie.
Le développement de nodules au niveau de la thyroïde est très fréquent, sous forme liquide (kystes) ou solide. Ces nodules thyroïdiens sont généralement bénins, avec seulement 10 à 15 % des nodules qui sont de nature cancéreuse. Le cancer de la thyroïde survient environ trois fois plus chez la femme que chez l’homme, et l’incidence de ce cancer varie d’un pays à l’autre : par exemple, en 2012, les taux de cancers thyroïdiens pour 100 000 femmes étaient de 89 en Corée du Sud, 20 aux États-Unis, 15 en Italie, 13 en France, 8 en Finlande et 6,5 au Japon. Il est très rare avant l’âge de 15 ans et représente moins de 1 % de l’ensemble des cancers de l’enfant.
Il existe plusieurs types de cancer de la thyroïde :
- Les cancers différenciés (papillaires ou folliculaires) : les cancers papillaires sont les plus fréquents, représentant environ 80 % des cancers de la thyroïde. Ils sont principalement diagnostiqués entre 30 et 50 ans et sont de bon pronostic. Les cancers folliculaires représentent environ 10 % des cancers de la thyroïde. Ils sont généralement peu agressifs et de progression lente ;
Les cancers indifférenciés (anaplasiques) : ils surviennent principalement chez les personnes âgées (environ 1 % des cancers thyroïdiens), le pronostic est très sombre, avec une espérance de vie de l’ordre de quelques mois ;
- Les cancers médullaires (familiaux) : le pronostic des cancers médullaires est plus réservé avec une survie de 65 % 10 ans après le diagnostic.
En général, le processus de diagnostic d’un cancer de la thyroïde débute lorsqu’un patient présente des symptômes évocateurs de cette maladie ou que des nodules sont détectés fortuitement lors d’un examen clinique de routine.
La réalisation d’un dépistage systématique par échographie dans une population qui ne présente pas de signes cliniques évocateurs d’un cancer de la thyroïde peut révéler des cancers thyroïdiens qui n’auraient pas progressé (généralement de très petite taille) et n’auraient jamais été diagnostiqués en l’absence de dépistage. En effet, le cancer de la thyroïde a la particularité de progresser généralement lentement et ne provoque des symptômes que lorsqu’il est à un stade avancé. Ces cancers diagnostiqués lors d’un dépistage correspondent à ce que les cancérologues appellent des cancers indolents ou quiescents. La détection précoce de ces nodules cancéreux n’améliore ni la santé ni la survie des patients, mais peut au contraire altérer leur qualité de vie à cause d’un traitement médical et/ou de complications chirurgicales. Le dépistage du cancer de la thyroïde entraîne donc un surdiagnostic des cancers thyroïdiens, c’est-à-dire une détection de cas pour lesquels les risques l’emportent sur les bénéfices (Togawa et al. Lancet Oncol 2018).
La glande thyroïde est un organe particulièrement sensible aux rayonnements ionisants, en particulier après une exposition dans l’enfance. Chez des individus exposés aux rayonnements ionisants durant l’enfance, le risque de survenue d’un cancer thyroïdien varie selon le type d’exposition (irradiation externe ou interne), le type histologique de cancer thyroïdien (papillaire, folliculaire), l’âge à l’exposition, le temps écoulé depuis l’exposition, la présence d’une carence en iode, etc. L’augmentation de ce risque peut être très élevée, pouvant aller jusqu’à un risque multiplié par 20 pour une dose à la thyroïde de 1 Gy après irradiation externe d’après certaines études épidémiologiques.
2.1.2. Peut-on reconnaître un cancer radio-induit ?
Face à un cancer de la thyroïde, il n’existe pas de critères cliniques ou anatomopathologiques spécifiques permettant de déterminer si son développement est spontané ou dû aux conséquences de l’exposition aux radiations. Les cancers spontanés, comme ceux développés après exposition aux rayonnements ionisants, sont majoritairement des cancers différenciés de type papillaire (PTC), de bon pronostic. Il n’existe pas non plus d’altérations géniques (mutations, altération de gènes, etc.) spécifiques de l’exposition aux radiations.
Pour cette raison, plusieurs équipes ont recherché des groupes de marqueurs moléculaires (signatures) qui permettraient de distinguer les tumeurs spontanées de celles développées après exposition à l’iode 131 principalement au niveau du transcriptome (expression des gènes) et du miRNome (expression des petits ARN non codants). De telles signatures ont été identifiées dans certaines études (Detours et al. 2007, Port et al. 2007, Ugolin et al. 2011), mais pas dans d’autres (Detours et al. 2005, Dom et al. 2012, Morton et al. 2021), avec très peu de recouvrement entre elles en termes de marqueurs identifiés.
Une raison pouvant expliquer ces divergences réside dans la difficulté de définir un groupe de tumeurs radio-induites (i.e. dont le développement est dû à l’exposition à coup sûr) en raison de l’absence de critères objectifs pour les identifier. Le seul paramètre pouvant aider à définir ce groupe de tumeurs radio-induites est une forte dose à la thyroïde car l’épidémiologie montre une augmentation du risque de développer un cancer radio-induit avec la dose. De plus, l’estimation de la dose à la thyroïde pour les individus dont les PTC ont été diagnostiqués après l’accident de Tchernobyl n’a été disponible qu’en 2012 (Likhtarov et al. 2013). Il est vraisemblable que, dans le groupe de tumeurs radio-induites, les études antérieures aient intégré des tumeurs associées à des niveaux de doses très hétérogènes. Ainsi, certaines tumeurs associées aux plus faibles doses avaient une faible probabilité d’être véritablement radio-induites. C’est dans cet esprit qu’une étude a comparé le transcriptome de tumeurs de sujets non exposés avec celui de sujets traités pendant l’enfance par une radiothérapie avec une dose à la thyroïde de 10 à 40 Gy (avec une forte probabilité d’être véritablement radio-induites). Une signature de 322 gènes a été identifiée et validée sur une série indépendante de tumeurs (Ory et al. 2011, Ory et al. 2013).
Il est également vraisemblable que, parmi les PTC post-Tchernobyl étiquetés « radio-induits », certains étaient des cancers spontanés subcliniques déjà présents chez l’individu au moment de l’accident et révélés par un dépistage systématique dans la population exposée.
Les études réalisées à ce jour ont majoritairement considéré les tumeurs. Cependant, une étude a comparé le transcriptome de tissus sains thyroïdiens chez des Ukrainiens exposés ou non à l’iode 131 et a identifié une signature suggérant l’existence d’une « mémoire moléculaire » de l’exposition à long terme, indépendante de la carcinogenèse (Dom et al. 2012). Ainsi, les signatures moléculaires précédemment identifiées pourraient présenter un mélange de marqueurs d’exposition et de carcinogenèse.
En conclusion, à ce jour, l’existence d’une signature moléculaire des tumeurs radio-induites de la thyroïde reste soumise à débat. De nouvelles études sont nécessaires pour préciser l’effet du contexte d’exposition (dose, débit de dose) sur les spécificités des tumeurs développées. Il est nécessaire de revisiter la stratégie d’identification des signatures des tumeurs de la thyroïde en tenant compte de la signature d’exposition pour isoler la composante « carcinogénèse » et proposer un outil d’épidémiologie moléculaire de ces tumeurs.
2.1.3. Risque de cancer de la thyroïde dû aux retombées radioactives de l’accident de Tchernobyl
Dès le début des années 1990, des médecins pédiatres de Biélorussie et d’Ukraine ont constaté une augmentation importante du nombre de cancers de la thyroïde, principalement de type papillaire, chez des enfants et adolescents exposés aux retombées radioactives après l’accident de Tchernobyl. Par la suite, de nombreuses études ont montré que cette hausse était principalement due aux iodes radioactifs relâchés durant l’accident, l’incidence de ce cancer augmentant avec la dose de rayonnement à la thyroïde.
Afin de mieux caractériser l’augmentation du risque de cancer de la thyroïde suite à l’exposition aux iodes radioactifs, un dépistage de la thyroïde comprenant une imagerie par ultrasons et un examen clinique a été mis en place pour environ 13 000 enfants en Ukraine et 12 000 en Biélorussie (âgés de 18 ans ou moins en 1986) chez qui des mesures directes de l’activité radiologique thyroïdienne avaient pu être réalisées dans les 2 mois qui ont suivi l’accident de Tchernobyl. Ces dépistages ont été effectués plus de 10 ans après l’accident, une fois que l’augmentation de l’incidence du cancer de la thyroïde avait été bien établie chez les jeunes âgés de 18 ans ou moins au moment de l’accident.
En Russie, un examen clinique annuel réalisé sur la population, complété par une échographie ou d’autres procédures d’imagerie si nécessaire, a été mis en place en 1991 parmi les 110 000 résidents des régions les plus contaminées âgés de moins de 18 ans au moment de l’accident.
L’ensemble de ces études a montré une augmentation significative du risque de cancer de la thyroïde chez les personnes exposées aux retombées radioactives dans l’enfance et l’adolescence, avec un risque multiplié par 2,5 à 6 pour une dose de 1 Gy selon les études. Elles ont également permis d’estimer la part respective du dépistage et de l’exposition aux rayonnements ionisants dans l’augmentation du risque de cancer de la thyroïde.
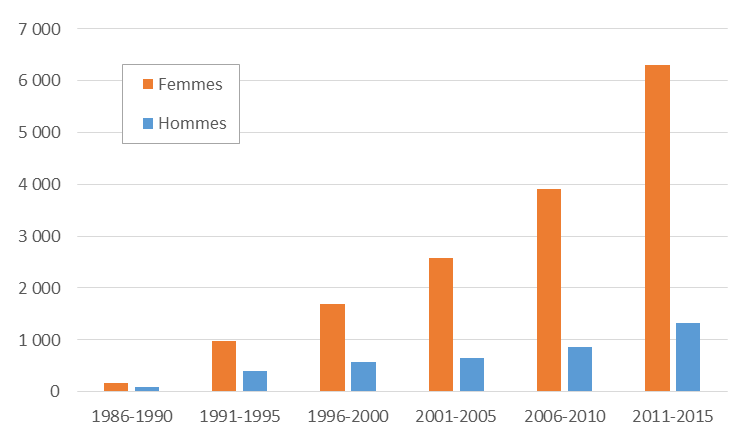
D’après le bilan sur le cancer de la thyroïde en Ukraine, Biélorussie et dans les régions les plus contaminées de Russie, publié en 2018 par le Comité scientifique des Nations Unies pour l’étude des effets des rayonnements ionisants (UNSCEAR 2018), environ 20 000 cas de cancer thyroïdien ont été diagnostiqués sur la période 1991-2015 chez les personnes âgées de moins de 18 ans au moment de l’accident, soit presque 3 fois plus que sur la période 1991-2005. Sur la dernière période 2011-2015, 7 630 nouveaux cas ont été diagnostiqués au total, dont 80 % de femmes. Cette augmentation au cours du temps de l’incidence du cancer de la thyroïde chez les moins de 18 ans au moment de l’accident est attribuable à la hausse des taux de base de cancer avec l’âge (le risque de cancer augmentant spontanément avec l’âge), à l’exposition aux rayonnements ionisants et à l’amélioration des méthodes de détection médicale. L’UNSCEAR a estimé qu’environ 25 % de ces cancers de la thyroïde, soit environ 5 000 cas, étaient attribuables à l’exposition aux rayonnements ionisants (entre 7 % et 50 % étant donné les incertitudes).
D’après une étude publiée en 2025 sur des données issues du registre de cancer en Biélorussie, il est probable qu’un risque légèrement accru de développer un cancer de la thyroïde associé à une exposition à l’iode 131 soit toujours présent à l’avenir chez les enfants exposés entre 0 et 6 ans, mais la proportion de ces cancers diminuera progressivement avec le vieillissement de cette cohorte (Fridman et al. 2025).
Une question importante à la suite de l’accident de Tchernobyl était de savoir si l’exposition à l’iode 131 pouvait également entraîner un risque accru de cancer de la thyroïde chez les personnes exposées à l’âge adulte (Hatch et al. 2017). Des augmentations de l’incidence du cancer de la thyroïde ont été observées parmi les travailleurs russes (Ivanov et al. 2008) et baltes (Rahu et al. 2013), en particulier parmi ceux ayant travaillé dans les premiers mois après l’accident, lorsque l’exposition à l’iode radioactif pouvait se produire. Une étude sur les cohortes de liquidateurs biélorusses, russes et baltes (Kesminiene et al. 2012), utilisant une reconstruction de doses individuelles, a également trouvé une augmentation du risque de cancer de la thyroïde. Le risque était multiplié par 5 pour une dose de 1 Gy reçue à la thyroïde et cette augmentation ne pouvait s’expliquer uniquement par les campagnes de dépistage thyroïdien et l’attention accrue des professionnels de santé vis-à-vis de cette pathologie chez les liquidateurs.
De nombreuses études ont été publiées donnant chacune des estimations différentes sur le nombre de cas de maladies ou de décès liés directement à l’exposition aux rayonnements ionisants dus à l’accident de Tchernobyl. Certaines conséquences sanitaires sont bien connues et avérées (comme le cancer de la thyroïde après exposition durant l’enfance), tandis que d’autres présentent des incertitudes avec des estimations qui peuvent varier selon la méthode appliquée : observation de cas recensés après l’accident (cf. Chapitres 1 et 2.1), études épidémiologiques post-Tchernobyl (cf. Chapitres 2.1.3 et 2.2), ou projection de risque dans différentes populations. Ceci a fait l’objet d’une note de synthèse publiée en juin 2025 sur le site de la Commission Nationale du Débat Public (Productions du Comité de la donnée | CNDP).
Les projections de risque ont pour objectif d’estimer, par calcul, le nombre de cas de maladies ou de décès attribuables à une exposition aux rayonnements ionisants, dans une population donnée, pendant une période donnée. Pour réaliser une projection de risque, on a besoin d’une estimation des doses, d’un modèle de relation dose-risque et de taux de base de cancer dans la population considérée. Il s’agit d’une estimation par calcul, et non d’une observation épidémiologique. Les résultats sont dépendants des paramètres utilisés pour le calcul de prédiction (période de prédiction considérée, taille de la population, zone géographique, niveau des doses estimées, etc.) et peuvent être interprétés ou comparés seulement en connaissant ces paramètres. Les résultats ainsi obtenus sont associés à des incertitudes importantes (reflétées par la largeur des « intervalles de confiance (IC) ») et doivent être considérés comme une indication d’un ordre de grandeur du risque.
Le risque de cancer attribuable aux retombées radioactives de l’accident de Tchernobyl en Europe
A la suite de l’accident de Tchernobyl, plusieurs projections de risque ont été effectuées par différents auteurs. En 2006, un calcul de projection du risque de cancer consécutif à l’accident de Tchernobyl a été réalisé pour l’ensemble de l’Europe (Cardis et al. 2006). Pour cela, les auteurs ont utilisé des estimations actualisées des doses dues à l’accident (doses moyennes spécifiques à chaque pays/région, reçues au corps entier et à la thyroïde), des modèles de risque dérivés de l’étude épidémiologique des survivants des bombardements atomiques de Hiroshima et Nagasaki, et des données sur les taux de cancer dans les différents pays européens. Ces projections de risque prévoient que, sur l’ensemble des cas de cancer qui devraient survenir en Europe entre 1986 et 2065 (c’est-à-dire 80 ans après l’accident de Tchernobyl), environ 0,01 % pourraient être liés aux retombées radioactives de l’accident. Ainsi, il est estimé qu’environ 16 000 (IC à 95 % : 3 400-72 000) cas de cancer de la thyroïde (dont environ 7 000 dans les trois zones les plus contaminées) et 25 000 (IC à 95 % : 11 000-59 000) cas d’autres cancers (dont environ 6 000 dans les trois zones les plus contaminées) pourraient survenir dans l’ensemble de l’Europe en raison des retombées radioactives de l’accident, comparativement à plusieurs centaines de millions de cas de cancer qui seraient dus à d’autres causes pendant la même période.
Le risque de cancer de la thyroïde attribuable aux retombées radioactives de l’accident de Tchernobyl en France
En 2000, une étude de l’IRSN et de l’Institut national de Veille Sanitaire (aujourd’hui Santé publique France) a estimé le nombre de cancers de la thyroïde sur la période 1991-2007 attribuables aux retombées radioactives de l’accident de Tchernobyl parmi les 2,3 millions d’enfants de moins de 15 ans résidant dans l’Est de la France en 1986. L’estimation aboutissait à un faible nombre de cancers de la thyroïde théoriquement attribuables aux retombées radioactives de l’accident : entre 5 et 63 cas en excès (Catelinois et al. 2005).
Cette estimation était du même ordre de grandeur que l’incertitude associée au nombre attendu de cancers de la thyroïde en l’absence d’exposition accidentelle à l’iode 131 au sein de cette population (environ 900 ± 60 cas spontanés).
Ce constat s’explique par le niveau des doses dues aux retombées de l’accident de Tchernobyl en France (de l’ordre de 100 fois moins que celles reçues par les enfants de Biélorussie parmi lesquels une augmentation du nombre de cancers thyroïdiens a été décelée). L’étude concluait qu’un tel excès de cas serait très difficilement détectable par une étude épidémiologique (Rogel et al. 2016).
2.1.4. Risque de cancer de la thyroïde après l’accident de Fukushima
Peu de temps après l’accident de la centrale nucléaire de Fukushima Daiichi en 2011, sur la base du retour d’expérience de l’accident de Tchernobyl, le gouvernement japonais a lancé un vaste programme de surveillance sanitaire nommé « Fukushima Health Management Survey ». Il inclut la mise en place d’un dépistage systématique du cancer de la thyroïde par échographie pour les 300 000 jeunes qui résidaient dans la préfecture de Fukushima au moment de l’accident.
Depuis 2014, des bilans thyroïdiens de suivi sont réalisés tous les 2 ans chez les jeunes âgés de moins de 20 ans, puis tous les 5 ans au-delà de cet âge. Comparativement à Tchernobyl, les doses de rayonnements à la thyroïde chez les jeunes à Fukushima ont été plus faibles, de l’ordre de quelques mGy, avec une dose à la thyroïde maximale d’environ 60 mGy chez les enfants, soit 10 à 100 fois moins que les doses reçues après Tchernobyl.
Le dépistage systématique mis en place dans la préfecture de Fukushima montre un nombre élevé de nodules tumoraux de la thyroïde chez les enfants âgés de 18 ans ou moins au moment de l’accident. Les fréquences de nodules tumoraux sont de l’ordre de :
- 39/100 000 dans la première campagne de dépistage (prévalence de 116 cas) ;
- 9/100 000 par an dans la deuxième campagne (incidence de 71 nouveaux cas en 2 ans) ;
- 7/100 000 par an dans la troisième campagne (incidence de 31 nouveaux cas en 2 ans) ;
- 11/100 000 par an dans la quatrième campagne (incidence de 39 nouveaux cas en 2 ans) ;
- Environ 10/100 000 par an dans la cinquième campagne, prolongée de 2 à 3 ans en raison de la pandémie de Covid-19 (incidence de 48 nouveaux cas en 4 ans) ;
- La sixième campagne de dépistage est en cours, avec une incidence de 11 nouveaux cas pour le moment, selon le rapport de l’Université de Médecine de Fukushima (FMU) publié en février 2025.
Pour les deux dernières campagnes, le nombre de cas n’est pas encore consolidé et est susceptible d’augmenter.
Interprétation des résultats du dépistage thyroïdien dans la préfecture de Fukushima :
Il faut faire la distinction entre la prévalence et l’incidence de nodules ou cancers de la thyroïde. La prévalence correspond à la fréquence de personnes atteintes d’une maladie à un moment donné, incluant à la fois les nouveaux cas et les anciens cas. L’incidence correspond à la fréquence de nouveaux cas d’une maladie sur une période donnée.
Dans le cadre du dépistage systématique dans la préfecture de Fukushima, la première campagne de dépistage d’octobre 2011 à mars 2014 fournit des données de prévalence : de ce fait, certains nodules identifiés pouvaient être déjà présents chez les individus avant l’accident en mars 2011. Par contre, la deuxième campagne de dépistage et toutes les campagnes suivantes fournissent des données d’incidence : seuls les nouveaux cas survenus depuis la campagne de dépistage précédente sont identifiés. Les résultats de la deuxième campagne et des campagnes suivantes ne peuvent donc pas être comparés directement à ceux de la première campagne. Dans le cas de maladies évoluant lentement, ce qui est le cas du cancer de la thyroïde, la prévalence est supérieure à l’incidence.
La plupart des cas identifiés par le dépistage systématique dans la préfecture de Fukushima sont des nodules tumoraux de petite taille, sans expression clinique, c’est-à-dire sans grosseur au cou détectable par palpation, et sans perturbation endocrinienne. Ces cas ne peuvent être comparés à ceux détectés par un registre de cancers qui enregistre essentiellement les cas cliniquement exprimés ou découverts fortuitement. La fréquence des nodules tumoraux détectés par une campagne de dépistage est donc naturellement très supérieure à celle fournie par un registre.
L’augmentation de la prévalence ou de l’incidence liée au caractère systématique d’un dépistage est appelé « facteur de dépistage ». Ainsi, la Corée du Sud a mis en place à partir de 1999 un dépistage du cancer de la thyroïde par échographie chez l’adulte : la comparaison des chiffres de 1993 à ceux de 2011 montre que le taux observé de cancer thyroïdien a été multiplié par un facteur de 15 suite à la mise en place de ce dépistage (Ahn et al. 2016). Sur la base des résultats sur l’incidence de ce cancer après l’accident de Tchernobyl en Ukraine, il a été estimé que l’impact du dépistage par échographie thyroïdienne à Fukushima pourrait avoir entraîné une augmentation d’un facteur 7 par rapport au taux de référence prédit par un registre de cancer (Jacob et al. 2014).
Afin de rendre la comparaison pertinente, les données issues du dépistage mis en place dans la préfecture de Fukushima doivent être comparées à celles obtenues dans une campagne de dépistage dans des zones non exposées, en utilisant le même protocole d’examen que dans la préfecture de Fukushima. Ainsi, au cours de la période 2011-2014, des campagnes de dépistage systématique du cancer de la thyroïde similaires à celle de Fukushima ont été mises en place chez des enfants âgés de 18 ans ou moins dans trois préfectures japonaises non touchées par l’accident (préfectures d’Aomori, Hiroshima et Yamanashi). Les données issues de ces campagnes montrent que la prévalence de nodules thyroïdiens de taille supérieure à 5 mm ou de kystes de plus de 20 mm détectés chez les jeunes par échographie dans ces préfectures était similaire à la prévalence observée dans la préfecture de Fukushima (Shimura et al. 2022).
Les cancers de la thyroïde à Fukushima sont-ils dus aux retombées radioactives de l’accident ?
À ce stade, étant donné l’effet du dépistage et les différences entre prévalence et incidence, il est encore prématuré de se prononcer sur une éventuelle augmentation des cancers de la thyroïde consécutive à l’accident chez les enfants présents en 2011 dans la préfecture de Fukushima lors de l’accident nucléaire.
À ce jour, plusieurs éléments indiquent que la fréquence élevée de nodules tumoraux thyroïdiens observés dans la préfecture de Fukushima est liée à l’effet du dépistage plutôt qu’à un effet des rayonnements (Cléro et al. Environ Int 2021 ; Cléro et al. Environ Risque & Santé 2021) :
- La distribution de l’âge des cas observés est proche de celle classiquement observée dans une population non exposée (alors que les cas observés après l’accident de Tchernobyl étaient beaucoup plus jeunes) ;
- Une étude parue en 2015 a analysé le profil oncogénique de 68 cas de cancer de la thyroïde identifiés et opérés dans le cadre du dépistage systématique de la préfecture de Fukushima (Mitsutake et al. 2015) : la fréquence des altérations génétiques observées est similaire à celle observée dans une population non exposée (et très différente de celle observée après l’accident de Tchernobyl) ;
- La prévalence de nodules thyroïdiens observée dans la préfecture de Fukushima dans la première campagne de dépistage apparaît très proche de celle observée dans les préfectures d’Aomori, Hiroshima et Yamanashi non exposées aux rejets radioactifs de l’accident, dans lesquelles des campagnes de dépistage similaires ont été mises en place ;
- Plusieurs études de modélisation réalisées en se basant sur des données ukrainiennes, coréennes ou japonaises concluent que l’effet du dépistage est compatible avec la prévalence élevée de nodules thyroïdiens enregistrée dans la préfecture de Fukushima.
Les niveaux de doses estimés pour les enfants présents en 2011 dans la préfecture de Fukushima sont faibles pour la plupart d’entre eux. Très peu d’enfants ont pu recevoir des doses à la thyroïde dépassant quelques dizaines de mGy du fait de l’inhalation d’iode radioactif. Actuellement, les doses dues à une contamination interne des enfants n’ont pas été reconstituées individuellement. Mais, parmi les cas diagnostiqués pour lesquels la dose externe a été reconstituée, la dose estimée la plus élevée était de l’ordre de 2 mSv. L’UNSCEAR considère que les futurs effets sanitaires radio-induits (incluant une éventuelle augmentation de la fréquence des cancers de la thyroïde) seront difficilement discernables à Fukushima, étant donné le faible niveau d’exposition aux rayonnements ionisants (UNSCEAR 2022).
Quatre ans après l’accident de Fukushima, Tsuda et al. ont comparé les données issues des deux premières campagnes (l’une en prévalence et l’autre en incidence) aux données d’incidence annuelle des cancers de la thyroïde au niveau national au Japon, ainsi qu’à l’incidence dans une zone de la préfecture de Fukushima choisie comme référence (Tsuda et al. 2016). Les auteurs ont indiqué que le nombre de cancers observés était nettement supérieur au nombre attendu sur la base des données d’incidence nationales et régionales, et ont conclu que cette augmentation pouvait être attribuée à l’exposition aux rayonnements ionisants résultant de l’accident. Cette étude écologique a été vivement critiquée par de nombreux scientifiques du monde entier en raison de ses importantes limites en termes de méthodologie et d’interprétation des résultats, ne permettant pas de justifier une telle conclusion (Wakeford et al. 2016, Cléro et al. Environ Int 2021). À ce jour, les études épidémiologiques réalisées n’ont pas montré d’association entre la distribution spatiale des doses estimées à la thyroïde et la fréquence des cancers de la thyroïde dans la préfecture de Fukushima (Ohira et al. 2020).
Chez les travailleurs de la centrale de Fukushima Daiichi, la possibilité de survenue d’un cancer thyroïdien ne peut être exclue car une dizaine de travailleurs a reçu une dose absorbée à la thyroïde estimée entre 2 et 32 Gy. Toutefois, ce nombre de travailleurs exposés à ces fortes doses absorbées à la thyroïde est probablement trop faible pour pouvoir discerner une incidence accrue de ce cancer. Les résultats provisoires d’une enquête impliquant des examens par ultrasons de la thyroïde de 627 travailleurs d’urgence avec une dose absorbée à la thyroïde supérieure à 100 mGy et de 1 437 travailleurs avec une dose plus faible à la thyroïde ne montrent aucune différence significative de l’incidence des pathologies thyroïdiennes entre les deux groupes (IAEA 2015).
Dans le cadre d’un projet européen sur l’amélioration de la surveillance sanitaire et médicale après un accident nucléaire auquel l’IRSN a participé, le Consortium SHAMISEN (Nuclear Emergency Situations - Improvement of Medical And Health Surveillance : https://www.isglobal.org/en/-/shamisen) recommande d’envisager un dépistage sanitaire systématique après un accident nucléaire uniquement s’il est dûment justifié, c’est-à-dire en s’assurant que le dépistage fera plus de bien que de mal. En se basant sur l’expérience du dépistage dans la préfecture de Fukushima, le Consortium ne recommande pas le dépistage systématique du cancer de la thyroïde car les effets psychologiques et physiques négatifs seront probablement plus importants que les bienfaits éventuels dans les populations touchées. Cependant, le Consortium recommande qu’une surveillance sanitaire de la thyroïde soit mise à la disposition des personnes qui en font la demande, qu’elles présentent un risque de cancer accru ou non, accompagnée d’informations et d’un soutien appropriés (Cléro et al. Environ Int 2021).
Un travail spécifique sur l’intérêt du dépistage systématique du cancer de la thyroïde a également été réalisé en 2018 par un groupe d’experts coordonné par le Centre International de Recherche sur le Cancer (IARC, Thyroid monitoring after nuclear accident (TM-NUC) http://tmnuc.iarc.fr/en/), dont l’IRSN faisait partie. En cohérence avec les conclusions du Consortium SHAMISEN, ce groupe d’experts ne recommande pas de dépistage systématique du cancer thyroïdien par examen ultrasonographique après un accident nucléaire, notamment du fait du risque de surdiagnostic. Il recommande de privilégier une mise à disposition des moyens de dépistage pour des groupes d’individus à haut risque, associée à une information détaillée des risques liés au surdiagnostic auprès des patients et des familles (Togawa et al. Lancet Oncol 2018).
Après l’accident en 2011, la prise en charge clinique d’un nodule tumoral de la thyroïde dans la préfecture de Fukushima consistait quasi systématiquement en l’ablation chirurgicale complète ou partielle de la thyroïde. Cependant, ces dernières années, considérant que la plupart des nodules (même tumoraux) sont indolents et peuvent rester sans évolution durant de nombreuses années, les recommandations cliniques ont évolué vers une surveillance échographique des nodules ne présentant pas de critère de gravité. Aujourd’hui, la position des médecins de l’Université Médicale de Fukushima est d’aller vers un mode de dépistage et une prise en charge thérapeutique moins systématique. En particulier, ils conseillent de limiter la réalisation d’opérations chirurgicales lors du diagnostic, et de proposer de façon plus large un suivi individuel permettant de surveiller l’évolution des nodules détectés (recommandation d’une approche « wait and see »). D’autres mesures ont été prises pour réduire les inconvénients du dépistage, telles qu’un accompagnement psychologique proposé aux personnes ayant eu des examens complémentaires afin de répondre à leurs inquiétudes (équipe de soutien, ligne téléphonique dédiée, aide financière pour les frais médicaux liés au traitement, etc.). Concernant la communication, une brochure intitulée « Avantages et inconvénients de l’examen » est distribuée aux participants car il est important qu’ils comprennent les avantages et les inconvénients de l’échographie thyroïdienne avant de prendre une décision éclairée quant à leur participation au dépistage. Des séances d’information sont également réalisées dans des collèges et lycées de la préfecture de Fukushima, et une vidéo d’animation explicative est diffusée dans divers lieux ou établissements publics dans lesquels des examens thyroïdiens sont réalisés.
En 2011, la préfecture de Fukushima ne disposait pas d’un registre des cancers. Si cela avait été le cas, elle aurait pu utiliser ce suivi pour quantifier l’incidence des cancers avant et après l’accident, et ainsi repérer une éventuelle recrudescence des cancers de la thyroïde. Le projet SHAMISEN recommande la mise en place de registres du cancer, qui aident à estimer le risque sanitaire et à dialoguer avec la société civile en cas d’accident nucléaire. La France s’est dotée d’un registre national des cancers de l’enfant (RNCE) à la fin des années 1990. Pour les adultes, un registre national des cancers (RNC) est en cours d’élaboration depuis décembre 2025, sur la base d’un système hybride combinant les données des registres de cancers du réseau Francim et les données médico-administratives du système national des données de santé (SNDS).
2.2 Autres cancers et effets non cancéreux après un accident nucléaire
2.2.1. Risques sanitaires pour les intervenants après un accident nucléaire
Accident de la centrale de Tchernobyl :
Des études s’appuyant sur une reconstruction individuelle détaillée de la dose reçue à la moelle osseuse ont montré une augmentation du risque de leucémie en fonction de la dose estimée chez les liquidateurs des pays baltes, de Biélorussie, de Russie et d’Ukraine, y compris pour la leucémie lymphoïde chronique généralement considérée comme non radio-induite (Kesminiene et al. 2008, Romanenko et al. 2008, Zablotska et al. 2013). En Ukraine, une augmentation de l'incidence du myélome multiple et du syndrome myélodysplasique a également été observée chez les liquidateurs par rapport à la population générale, mais ces résultats sont à considérer avec prudence car la dose n’a pas été prise en compte dans l’analyse (Bazyka et al. 2013).
Enfin, une augmentation de l’incidence des cancers solides liée à la dose chez les travailleurs russes figurant dans le registre national de Tchernobyl a été observée (Kashcheev et al. 2015). Bien que l'exhaustivité de l’identification des cas soit incertaine pour cette cohorte, cette observation est complétée par une augmentation similaire de la mortalité due aux cancers solides, un résultat pour lequel il n’y a pas de biais de surveillance possible. Le risque de cancers solides estimé est cohérent avec celui obtenu dans des études récentes sur les travailleurs de l'industrie nucléaire (Richardson et al. 2015) et compatible avec les extrapolations des études sur les survivants des bombardements atomiques d’Hiroshima et Nagasaki (Ozasa et al. 2012).
Dans le cadre des études épidémiologiques réalisées en collaboration entre l’Ukraine et les Etats-Unis, l’irradiation externe lors des opérations de décontamination était la principale voie d’exposition pour la plupart des liquidateurs. Les doses de radiation correspondantes ont été estimées avec la méthode RADRUE (Realistic Analytical Dose Reconstruction with Uncertainty Estimation) qui fournit des estimations de dose pouvant être utilisées dans les études épidémiologiques avec un degré de fiabilité raisonnable. Les incertitudes dans les estimations des doses comprenaient deux éléments : 1) les incertitudes liées aux paramètres utilisés dans l’évaluation de l’exposition et liées au manque de connaissances sur les valeurs réelles des paramètres, et 2) les incertitudes liées au facteur humain en raison de problèmes de mémoire, entraînant des réponses incomplètes, inexactes ou manquantes lors des entretiens individuels réalisés longtemps après l’exposition des liquidateurs (Drozdovitch et al. 2024).
Accident de la centrale de Fukushima Daiichi :
Étant donné que la majorité des travailleurs a été faiblement exposée, avec des doses efficaces inférieures à 10 mSv au cours de la première année, et que moins de 1 % des travailleurs a reçu une dose efficace de 100 mSv ou plus au cours de la première année, il est peu probable qu'une augmentation de l'incidence des cancers (cancers solides, leucémies) due aux rayonnements ionisants soit perceptible.
En réponse aux préoccupations concernant les effets potentiels à long terme de l'exposition aux radiations sur la santé des travailleurs, une étude de cohorte (nommée NEWS, Nuclear Emergency Workers Study) a été lancée en 2014 pour fournir une évaluation complète de la santé des travailleurs intervenus sur le site de Fukushima Daiichi après l’accident (https://www.news.johas.go.jp/).
Environ 19 700 intervenants d’urgence (enregistrés dans la base de données du ministère de la Santé et du Travail) ont été invités à participer à l’étude NEWS. En novembre 2025, environ 8 500 travailleurs avaient donné leur consentement et 6 500 avaient complété l’enquête de base comprenant un auto-questionnaire et des examens médicaux (avec échantillons biologiques : sang et urine). Les enquêtes de suivi, initialement menées tous les 4-5 ans, sont réalisées tous les 2 ans depuis 2024. Le nombre d’établissements médicaux effectuant des examens de santé est passé à l’échelle nationale, avec environ 60 établissements au début de l’étude puis 240 sur l’ensemble du Japon.
Des dépistages spécifiques sont réalisés pour la cataracte, les troubles thyroïdiens et la santé mentale. Les doses individuelles de radiation sont en cours de reconstitution et permettront d’analyser les relations dose-risque en termes de mortalité et d’incidence (Kitamura et al. 2018 ; Yasui 2016).
2.2.2. Les pathologies non-cancéreuses pour les populations et intervenants exposés
Pathologies cardiovasculaires et cérébrovasculaires :
Les pathologies de l’appareil circulatoire associées à des expositions aux rayonnements ionisants sont principalement des cardiopathies ischémiques et des maladies cérébrovasculaires majoritairement causées par l’athérosclérose qui se caractérise par le dépôt d’une plaque essentiellement composée de lipides (athérome) sur la paroi des artères. À terme, ces plaques peuvent entrainer des lésions de la paroi artérielle (sclérose), conduire à l’obstruction du vaisseau ou encore se rompre, avec des conséquences telles qu’un infarctus aigu du myocarde ou un accident vasculaire cérébral (Tapio et al. 2021).
En 2006, un risque accru de maladie cérébrovasculaire et de cardiopathie ischémique lié à la dose de rayonnements ionisants a été observé chez les liquidateurs russes (Ivanov et al. 2006), bien qu’aucune information n’ait été disponible pour tenir compte d’autres facteurs de risque de ces maladies. Le suivi épidémiologique de ces liquidateurs, basé sur le registre national de Tchernobyl, a été prolongé de 12 ans, jusqu’en 2012, confirmant l’augmentation de l’ordre de 50 % par Gy du risque de maladie cérébrovasculaire (Kashcheev et al. 2016) ; là encore, aucune information n’était disponible sur les autres facteurs de risque, à l’exception des maladies concomitantes telles que le diabète. Une étude sur les liquidateurs ukrainiens intervenus sur la période 1986-1987 a aussi révélé une augmentation du risque de maladies cardiovasculaires et cérébrovasculaires liée à la dose (Krasnikova et al. 2013, Krasnikova et al. 2014). Cependant, ces résultats doivent être confirmés car on peut s’interroger sur l’exhaustivité et l’exactitude de l’enregistrement de ces maladies et des estimations de dose, et bien qu’un certain nombre de risques non liés aux rayonnements aient été identifiés, les facteurs de confusion n’ont pas été pris en compte, à l’exception de l’âge.
Une étude publiée en 2018 s’est intéressée au risque d’arythmie cardiaque chez des enfants vivant en territoires russes contaminés par les retombées de l’accident de Tchernobyl. Cette étude a été menée dans le cadre du programme de recherche EPICE (Evaluations des Pathologies Induites par le Césium), lancé par l’IRSN en 2009 en partenariat avec le centre de diagnostic clinique et biologique de la région de Bryansk (Russie), pour répondre aux questionnements de scientifiques et d’associations de riverains quant aux conséquences sanitaires de l’accident de Tchernobyl sur les enfants. Pendant quatre ans (2009-2013), environ 18 000 enfants (8 816 enfants en territoire contaminé, correspondant à un dépôt de césium 137 dans le sol > 555 kBq/m², et 8 881 enfants en territoire non contaminé, correspondant à un dépôt de césium 137 dans le sol < 37 kBq/m²), âgés de 2 à 18 ans ont été examinés sur le plan cardiaque et radiologique : électrocardiogramme, échographie cardiaque et mesure de l’activité corporelle en césium 137. Une irrégularité du rythme cardiaque (arythmie cardiaque légère et souvent bénigne) a été diagnostiquée chez environ 2 500 enfants, sans différence de prévalence entre les enfants des territoires contaminés et ceux des territoires non contaminés (13 % vs 15 %). De plus, le risque d’arythmie cardiaque n’augmentait pas avec la contamination corporelle en césium 137 des enfants. Ainsi, cette étude n’a pas observé d’association entre la contamination par le césium 137 et le risque d’arythmie cardiaque chez l’enfant (Jourdain et al. 2018).
Cataractes :
Les cataractes sont la cause la plus fréquente de cécité dans le monde. L’exposition aux rayonnements ionisants du cristallin est un facteur de risque connu d’apparition de cataractes chez l’humain. Les autres facteurs de risque sont le vieillissement, la génétique (cataractes congénitales), l’exposition aux ultraviolets, le diabète, un indice de masse corporelle élevé, le tabagisme, la consommation d’alcool, l’utilisation prolongée de corticostéroïdes et les traumatismes oculaires.
Un risque accru de cataracte, en particulier d’opacité cristallinienne sous-capsulaire postérieure, a été rapporté dans une cohorte de liquidateurs ukrainiens (Worgul et al. 2007). Cependant, les études menées jusqu’à présent ne permettent pas de conclure quant à un risque de cataracte significativement plus élevé en raison de problèmes méthodologiques liés à l’analyse statistique des données (Ainsbury et al. 2021).
Des données sur la fréquence des cataractes dans la population infantile de la région de Bryansk en Russie ont également été collectées dans le cadre du programme de recherche EPICE, mais en raison du contexte géopolitique, les analyses statistiques n’ont pas encore pu être menées à terme.
Pathologies thyroïdiennes non cancéreuses :
Les principales pathologies thyroïdiennes non cancéreuses comprennent d’une part les nodules bénins, dont l’adénome folliculaire, et d’autre part les dysfonctions thyroïdiennes hyper et hypothyroïdie, qui sont principalement d’origine auto-immune, en lien avec la production anormale d’anticorps antithyroïdiens.
A la suite de l’accident de Tchernobyl, ces pathologies ont été étudiées plus particulièrement dans deux cohortes d’enfants exposés avant l’âge de 18 ans, incluant environ 11 800 enfants en Ukraine et 10 800 en Biélorussie (Ostroumova et al. 2009 ; Ostroumova et al. 2013). Les doses moyennes à la thyroïde étaient de 0,79 Gy (max 40,8 Gy) et 0,54 Gy (max 26,6 Gy) dans les cohortes ukrainienne et biélorusse, respectivement.
Nodules thyroïdiens :
Bien que l’exposition infantile à l’iode 131 soit un facteur de risque établi pour le cancer de la thyroïde, les preuves d’une association avec les nodules thyroïdiens sont moins claires.
La prévalence de nodules bénins était significativement associée avec la dose reçue dans la cohorte biélorusse, ainsi qu’une augmentation significative de la prévalence d’adénomes folliculaires en Biélorussie et en Ukraine. Ce risque diminuait pour les enfants exposés à des âges plus avancés (Tronko et al. 2017). Cette hausse de prévalence de nodules bénins n’a pas été retrouvée dans une autre étude réalisée en Russie (Ivanov et al. 2005).
Dans une autre étude, 358 personnes présentant au moins un nodule thyroïdien ont été sélectionnées parmi plus 13 000 résidents ukrainiens âgés de moins de 18 ans au moment de l’accident de Tchernobyl. Une association significative a été observée entre l’exposition à l’iode 131 durant l’enfance et un risque accru de nodules thyroïdiens détectés 12 à 14 ans après l’exposition, avec un risque plus élevé pour les nodules néoplasiques versus non néoplasiques (Cahoon et al. 2024).
Plus récemment, une étude a été publiée sur un dépistage thyroïdien réalisé auprès de 1 439 biélorusses exposés avant leur naissance aux retombées radioactives de l’accident de Tchernobyl, pour lesquels les doses estimées à la thyroïde provenaient principalement de l’iode 131 (0,14 Gy en moyenne et 0,02 Gy en médiane). Cette étude a observé un risque significatif de nodules thyroïdiens bénins associé à l’exposition aux rayonnements ionisants au cours du troisième trimestre de grossesse (Mabuchi et al. 2026).
Dysfonction thyroïdienne :
L’incidence d’hypothyroïdie infraclinique (TSH > 4 mUi/l et hormones thyroïdiennes normales) était de 6,1 % et 2,8 % dans les cohortes ukrainienne et biélorusse, respectivement, alors qu’une hypothyroïdie clinique était retrouvée respectivement pour 0,1 et 0,2 % des enfants. Une association significative a été mise en évidence entre l’hypothyroïdie infraclinique et la dose reçue à la thyroïde dans ces deux cohortes, association similaire dans les deux sexes et ne variant pas significativement selon l’âge à l’exposition.
Pour ce qui concerne la relation dose-réponse entre la thyroïdite auto-immune et la dose reçue à la thyroïde, les résultats ne sont pas concluants, avec une augmentation significative en Biélorussie, mais pas en Ukraine ni en Russie (Agate et al. 2008 ; Ostroumova et al. 2009).
Sur un petit échantillon d’enfants exposés in utero (n=100), avec une dose moyenne à la thyroïde de 0,36 Gy, il n’a pas été mis en évidence d’hypothyroïdie, mais un plus petit volume de la thyroïde et une valeur de TSH plus élevée chez les enfants exposés au premier trimestre par rapport à ceux exposés au troisième trimestre (Drozd et al. 2003).
Aucun excès d’hypothyroïdie ni d’augmentation des anticorps antithyroïdiens n’ont été observés après l’accident de Fukushima. Les doses reçues étaient beaucoup plus faibles, inférieures à 5 mGy en moyenne (Watanobe et al. 2015).
Malformations congénitales :
Une augmentation ponctuelle de trisomie 21 a été observée en Biélorussie en janvier 1987, soit 9 mois après l’accident de Tchernobyl (Zatsepin et al. 2007). La relation de cause à effet n’a cependant pas été étudiée, donc il existe toujours des incertitudes sur un lien éventuel entre l’exposition aux rayonnements ionisants et le développement de malformations congénitales.
Un taux élevé d’anomalies congénitales (en particulier, anomalies du tube neural et microcéphalie) a été observé dans la région de Rivne au Nord-Ouest de l’Ukraine. Bien que l’exposition aux retombées de Tchernobyl soit très faible au regard du risque tératogène, des investigations complémentaires sont considérées nécessaires (Wertelecki 2021).
Effets cognitifs et neurologiques :
Il est désormais bien connu que des facteurs environnementaux et génétiques, des troubles psychiatriques tels que la schizophrénie et la dépression, et l’utilisation de certains médicaments peuvent jouer un rôle sur l’apparition de troubles neurologiques, cognitifs et du vieillissement, tels que la maladie d’Alzheimer et les démences séniles. Au cours des dernières années, l’étude des effets d’expositions à des rayonnements ionisants sur le développement neurologique et les fonctions cognitives a suscité un intérêt considérable. Cependant, la recherche dans ce domaine est encore rare (Pasqual et al. 2021).
Après l’accident de Tchernobyl, des études sur les liquidateurs ukrainiens exposés à une dose moyenne d’environ 100 mGy ont démontré une incidence accrue de dysfonctionnement cognitif, sans pour autant que la relation entre la nature des effets et la dose de rayonnement n’ait pu être établie de manière certaine (Loganovsky et al. 2008 ; Bazyka et al. 2018).
Dans le cadre du projet européen CEREBRAD (Cognitive and Cerebrovascular Effects Induced by Low Dose Ionizing Radiation), une étude menée auprès de 326 liquidateurs ukrainiens a montré une prévalence plus élevée de déficit cognitif et psychologique chez les travailleurs ayant reçu des doses supérieures à 100 mGy, en particulier chez ceux ayant reçu des doses supérieures à 500 mGy. Dans l’ensemble, cette étude suggère que le déficit cognitif chez l’homme, 25 à 30 ans après l’irradiation, pourrait être influencé par la dose et l’âge au moment de l’exposition.
Une augmentation des taux de pathologies neurologiques a également été observée dans un délai de 7 à 21 ans après l’exposition aux rayonnements ionisants dans une cohorte d’environ 40 000 personnes évacuées de la zone de Tchernobyl, en particulier 12 à 21 ans après l’exposition (Buzunov & Kapustynska 2018). Bien que les doses résultant d’une exposition externe et de la présence de radionucléides à vie longue soient relativement faibles, cette étude a montré une augmentation significative de la survenue de pathologies neurologiques chez les individus présentant des doses thyroïdiennes élevées d’iode 131, comprises entre 300 et 750 mGy. Toutefois, des études supplémentaires sont nécessaires afin de confirmer une éventuelle association entre la dose thyroïdienne et le développement d’un déficit cognitif chez les personnes exposées aux rayonnements.
Effets héréditaires :
Il existe des preuves convaincantes que les rayonnements ont des effets héréditaires (c’est-à-dire des effets chez les descendants de parents exposés aux rayonnements ionisants avant la conception) chez des animaux de laboratoire. Néanmoins à ce jour, aucune augmentation d’effets néfastes sur la santé n'a été constatée chez les enfants dont les parents ont été exposés à des rayonnements ionisants (Amrenova et al. 2021). Les mécanismes fondamentaux qui sous-tendent les effets intergénérationnels potentiellement liés aux rayonnements restent mal compris. Le risque de maladies liées aux rayonnements reste toutefois une préoccupation importante pour les personnes exposées aux rayonnements à la suite d’un accident nucléaire.
Une large étude, dite « de trios », basée sur un protocole combinant épidémiologie et génétique, a été réalisée sur des liquidateurs ukrainiens (Yeager et al. 2021). Les auteurs ont analysé le nombre total de mutations de novo (i.e. mutations de gène apparaissant chez un individu alors qu’aucun des parents ne la possède dans son patrimoine génétique) chez les enfants nés de parents qui ont été exposés en tant que travailleurs chargés du nettoyage de Tchernobyl en Ukraine ou évacués des zones contaminées dans un rayon de 70 km après l’accident de Tchernobyl. L’étude a inclus 130 enfants nés de 105 couples mère-père dont l’un des parents ou les deux avaient été exposés. La force de cette étude réside dans sa taille importante, son protocole bien conçu, sa méthode élaborée de reconstruction des doses cumulées au niveau des gonades par les parents avant la conception des enfants, et ses analyses statistiques adaptées à la détection d’une éventuelle relation dose-réponse. Les doses maternelles et paternelles ont été considérées séparément afin de considérer un éventuel effet du sexe. Les auteurs n'ont observé aucune évidence d’une relation dose-réponse, ni avec l’ensemble des mutations de novo, ni en considérant certains types spécifiques de mutations. Ils ont ainsi conclu que leurs résultats ne montraient aucune preuve d’un effet substantiel de l’exposition aux rayonnements ionisants sur les mutations germinales chez l’humain, et que donc, un impact héréditaire sur la santé des générations suivantes était improbable (Yeager et al. 2021).
2.3. Impact sanitaire non radiologique d’un accident nucléaire, notamment dû à l’évacuation
Les problèmes de santé suite à un accident nucléaire ne se limitent pas aux conséquences de l’exposition aux rayonnements ionisants.
Après l’accident de Fukushima Daiichi, le problème majeur au cours des premiers mois a été l’impact sanitaire de l’évacuation de la population locale, en particulier parmi les personnes les plus vulnérables telles que les personnes âgées. En effet, divers problèmes sont apparus à moyen et long terme suite à ce changement de mode de vie à grande échelle : défaillances des infrastructures et des services médicaux, isolement social, perte de motivation dans la vie, conflits entre générations, perturbation du régime alimentaire, entraînant des diagnostics et une prise en charge des maladies plus tardifs, l’aggravation de maladies chroniques comme le diabète et des problèmes psychologiques. L’apparition ou l’aggravation de ces problèmes sont aujourd’hui attribuées à un manque de soutien social et à des changements environnementaux plutôt qu’à la perception individuelle du risque lié à l’exposition aux rayonnements ionisants. La réorganisation des services de santé et la mise à disposition de ressources humaines et matérielles adéquates sont essentielles pour limiter les impacts négatifs sur la santé physique et mentale des populations touchées par un accident nucléaire (ICRP International Conference on Recovery After Nuclear Accidents, 2020 ; WHO 2020).
Une prise en compte équilibrée de ces différents risques sanitaires interconnectés et la mise en œuvre de contre-mesures à long terme sont donc nécessaires pour faire face aux conséquences sanitaires d’un accident nucléaire.
Plus de détails à ce sujet sont disponibles sur la note d’information « 15 ans après l’accident de la centrale de Fukushima Daiichi : Bilan de la surveillance sanitaire et des études épidémiologiques conduites chez les habitants de la préfecture de Fukushima et chez les travailleurs de la centrale nucléaire – Point de la situation en février 2026 ».
Agate L, et al. Thyroid autoantibodies and thyroid function in subjects exposed to Chernobyl fallout during childhood: evidence for a transient radiation-induced elevation of serum thyroid antibodies without an increase in thyroid autoimmune disease. J Clin Endocrinol Metab. 2008; 93: 2729-36.
Ahn HS, et al. Thyroid Cancer Screening in South Korea Increases Detection of Papillary Cancers with No Impact on Other Subtypes or Thyroid Cancer Mortality. Thyroid. 2016; 26(11): 1535-40.
Ainsbury EA, et al. Radiation-induced lens opacities: Epidemiological, clinical and experimental evidence, methodological issues, research gaps and strategy. Environ Int 2021; 146: 106213.
Amrenova A, et al. Intergenerational effects of ionizing radiation: review of recent studies from human data (2018-2021). Int J Radiat Biol. 2024; 100(9): 1253-63.
Bazyka DA, et al. Multiple myeloma among Chernobyl accident clean-up workers - state and perspectives of analytical study. Probl Radiat Med Radiobiol. 2013; 18: 169-72.
Bazyka D, et al. Epidemiology of Late Health Effects in Ukrainian Chornobyl Cleanup Workers. Health Phys. 2018; 115: 161-169.
Bogdanova TI, et al. Papillary Thyroid Carcinoma in Ukraine After Chernobyl and in Japan After Fukushima: Different Histopathological Scenarios. Thyroid. 2021; 31(9): 1322-34.
Buzunov OA, Kapustynska VO. Epidemiological studies of cerebrovascular disease of the population evacuated from the 306km zone of the ChNPP at the age of 18–60 years. Analysis of the influence of internal ionizing radiation on the thyroid gland 131I. Probl Radiac Med Radiobiol. 2018; 23: 96-106.
Cahoon EK, et al. Prevalence of Thyroid Nodules in Residents of Ukraine Exposed as Children or Adolescents to Iodine-131 from the Chornobyl Accident. Thyroid. 2024; 34(7):890-898.
Cardis E, et al. Cancer consequences of the Chernobyl accident: 20 years on. J Radiol Prot. 2006; 26(2):127-40.
Catelinois O, et al. Uncertainty and sensitivity analysis in assessment of the thyroid cancer risk related to Chernobyl fallout in Eastern France. Risk Anal. 2005; 25(2):243-52.
CEREBRAD. Cognitive and Cerebrovascular Effects Induced by Low Dose Ionizing Radiation. www.cerebrad-fp7.eu.
Cléro E, Leuraud K, Laurier D, Tsubokura M. Conséquences sanitaires 35 ans et 10 ans après les accidents nucléaires de Tchernobyl et de Fukushima. Environnement, Risques & Santé. 2021; 20(6), 525-534.
Cléro E, et al. Lessons learned from Chernobyl and Fukushima on thyroid cancer screening and recommendations in case of a future nuclear accident. Environ Int. 2021; 146: 106230.
Detours V. et al. Genome-wide gene expression profiling suggests distinct radiation susceptibilities in sporadic and post-Chernobyl papillary thyroid cancers. Br J Cancer. 2007; 97(6): 818-25.
Detours V. et al. Absence of a specific radiation signature in post-Chernobyl thyroid cancers. Br J Cancer. 2005; 92(8): 1545-52.
Dom G, et al. A gene expression signature distinguishes normal tissues of sporadic and radiation-induced papillary thyroid carcinomas. Br J Cancer. 2012; 107(6): 994-1000.
Drozd VM, et al. Screening of thyroid status in children exposed to ionizing radiation in utero and at the first year of life as a result of the Chernobyl accident. Int J Radiat Med. 2003; 5(1-2): 167-179.
Drozdovitch V, et al. Dose Reconstruction for Epidemiological Studies among Ukrainian Chernobyl Cleanup Workers. Radiat Res. 2024; 202(4):626-638.
FMU (Fukushima Medical University). Report of the Fukushima Health Management Survey (FY2024). February 2025.
Fridman M, Krasko O, Veyalkin I. The incidence trends of papillary thyroid carcinoma in Belarus during the post-Chernobyl epoch. Cancer Epidemiol. 2025; 95: 102745.
Hatch M, et al. Somatic health effects of Chernobyl: 30 years on. Eur J Epidemiol. 2017; 32(12): 1047-54.
IAEA. The Fukushima Daiichi accident. Technical volume 4. Radiological consequences. International Atomic Energy Agency, Vienna, 2015. https://www.iaea.org/publications/10962/the-fukushima-daiichi-accident
IARC Expert Group on Thyroid Health Monitoring after Nuclear Accidents. Thyroid health monitoring after nuclear accidents. IARC Technical Publications No 46. Lyon: IARC (International Agency for Research on Cancer), WHO; 2018. http://tmnuc.iarc.fr/en/
ICRP. International Conference on Recovery After Nuclear Accidents Radiological Protection Lessons from Fukushima and Beyond. 1-4 December, 2020. https://www.icrprecovery.org
Ivanov VK, et al. Non-cancer thyroid diseases among children in the Kaluga and Bryansk regions of the Russian Federation exposed to radiation following the Chernobyl accident. Health Phys. 2005; 88: 16-22.
Ivanov VK, et al. The risk of radiation-induced cerebrovascular disease in Chernobyl emergency workers. Health Phys 2006; 90: 199-207.
Ivanov VK, et al. Risk of thyroid cancer among Chernobyl emergency workers of Russia. Radiat Environ Biophys 2008; 47: 463-7.
Jacob P, Kaiser JC, Ulanovsky A. Ultrasonography survey and thyroid cancer in the Fukushima Prefecture. Radiat Environ Biophys. 2014; 53(2): 391-401. Erratum in: Radiat Environ Biophys. 2014; 53(2): 403.
Jourdain JR, et al. Is exposure to ionising radiation associated with childhood cardiac arrhythmia in the Russian territories contaminated by the Chernobyl fallout? A cross-sectional population-based study. BMJ Open. 2018; 8(3): e019031.
Kashcheev VV, et al. Incidence and mortality of solid cancer among emergency workers of the Chernobyl accident: assessment of radiation risks for the follow-up period of 1992–2009. Radiat Environ Biophys. 2015; 54: 13-23.
Kashcheev VV, et al. Radiation-epidemiological study of cerebrovascular diseases in the cohort of Russian recovery operation workers of the Chernobyl accident. Health Phys. 2016; 111: 192-7.
Kesminiene A, et al. Risk of hematological malignancies among Chernobyl liquidators. Radiat Res. 2008; 170: 721-35.
Kesminiene A, et al. Risk of thyroid cancer among Chernobyl liquidators. Radiat Res. 2012; 178: 425-36.
Kitamura H, et al. Epidemiological Study of Health Effects in Fukushima Nuclear Emergency Workers-Study Design and Progress Report. Radiat Prot Dosimetry. 2018; 182(1): 40-48.
Krasnikova LI, et al. Radiation and nonradiation factors impact on development of cerebrovascular diseases in the Chernobyl clean-up workers. The epidemiological study results. Probl Radiat Med Radiobiol. 2013; 18: 89-101.
Krasnikova LI, Buzunov VO. Role of radiation and non-radiation factors on the development of coronary heart disease in the Chernobyl clean-up workers: epidemiological study results. Probl Radiat Med Radiobiol. 2014; 19: 67-79.
Likhtarov I, et al. Reconstruction of individual thyroid doses to the Ukrainian subjects enrolled in the Chernobyl Tissue Bank. Radiat Prot Dosimetry. 2013; 156(4): 407-23.
Loganovsky K, et al. The mental health of clean-up workers 18 years after the Chernobyl accident. Psychol Med. 2008; 38(4): 481-488.
Mabuchi K, et al. Thyroid nodules after prenatal exposure to Chernobyl radioactive fallout in Belarus. Int J Radiat Biol. 2026; 102(1): 20-26.
Mitsutake N, et al. BRAF(V600E) mutation is highly prevalent in thyroid carcinomas in the young population in Fukushima: a different oncogenic profile from Chernobyl. Sci Rep. 2015; 5: 16976.
Morton LM, et al. Radiation-related genomic profile of papillary thyroid carcinoma after the Chernobyl accident. Science. 2021; 372(6543): eabg2538.
Ohira T, et al. Absorbed radiation doses in the thyroid as estimated by UNSCEAR and subsequent risk of childhood thyroid cancer following the Great East Japan Earthquake. J Radiat Res 2020. 61: 243-8.
Ory C, Ugolin N, Hofman P, Schlumberger M, Likhtarev IA, Chevillard S. Comparison of transcriptomic signature of post-Chernobyl and postradiotherapy thyroid tumors. Thyroid. 2013; 23(11): 1390-400.
Ory C, et al. Gene expression signature discriminates sporadic from post-radiotherapy-induced thyroid tumors. Endocr Relat Cancer. 2011; 18(1): 193-206.
Ostroumova E, et al. Subclinical hypothyroidism after radioiodine exposure: Ukrainian American cohort study of thyroid cancer and other thyroid diseases after the Chornobyl accident (1998–2000). Environ Health Perspect. 2009; 117: 745-50.
Ostroumova E, et al. Measures of thyroid function among Belarusian children and adolescents exposed to iodine-131 from the accident at the Chernobyl nuclear plant. Environ Health Perspect. 2013; 121: 865-871.
Oughton D, et al. on behalf of the SHAMISEN Consortium. Recommendations and procedures for preparedness and health surveillance of populations affected by a radiation accident. 2017. https://www.isglobal.org en/-/shamisen
Ozasa K, et al. Studies of the mortality of atomic bomb survivors, report 14, 1950-2003: An overview of cancer and noncancer diseases. Radiat Res. 2012; 177 (3): 229-243.
Pasqual E, et al. Cognitive effects of low dose of ionizing radiation - Lessons learned and research gaps from epidemiological and biological studies. Environ Int. 2021; 147: 106295.
Port M, Boltze C, Wang Y, Röper B, Meineke V, Abend M. A radiation-induced gene signature distinguishes post-Chernobyl from sporadic papillary thyroid cancers. Radiat Res. 2007; 168(6): 639-49.
Rahu K, et al. Site-specific cancer risk in the Baltic cohort of Chernobyl cleanup workers, 1986–2007. Eur J Cancer. 2013; 49: 2926-33.
Richardson DB, et al. Risk of cancer from occupational exposure to ionising radiation: retrospective cohort study of workers in France, the United Kingdom, and the United States (INWORKS). BMJ. 2015; 351: h5359.
Rogel A, et al. Épidémiologie du cancer de la thyroïde 30 ans après l’accident de Tchernobyl : fréquence, facteurs de risque et impact des pratiques diagnostiques. Bull Epidemiol Hebdo. 2016; 11-12: 200-5.
Romanenko AY, et al. The Ukrainian-American study of leukemia and related disorders among Chernobyl cleanup workers from Ukraine: III. Radiation risks. Radiat Res. 2008; 170: 711-20.
Shimura H, et al. Thyroid Ultrasound Examination Group. A Comprehensive Review of the Progress and Evaluation of the Thyroid Ultrasound Examination Program, the Fukushima Health Management Survey. J Epidemiol. 2022; 32(Suppl_XII): S23-S35.
Tapio S, et al. Ionizing radiation-induced circulatory and metabolic diseases. Environ Int 2021; 146: 106235.
Thomas G. Radiation and Thyroid Cancer – An Overview. Radiat Prot Dosimetry. 2018; 182(1): 53-57.
Togawa K, et al. Long-term strategies for thyroid health monitoring after nuclear accidents: recommendations from an Expert Group convened by IARC. Lancet Oncol. 2018; 19:(10): 1280-3.
Tronko MD, et al. Thyroid neoplasia risk is increased nearly 30 years after the Chernobyl accident. Int J Cancer. 2017; 141, 1585-88.
Ugolin N, et al. Strategy to find molecular signatures in a small series of rare cancers: validation for radiation-induced breast and thyroid tumors. PLoS One. 2011; 6(8): e23581.
UNSCEAR. Sources, effects and risks of ionizing radiation, United Nations Scientific Committee on the Effects of Atomic Radiation 2000 Report (Volume II) to the General Assembly with scientific annexes. Annex J: Exposures and effects of the Chernobyl accident. New York: United Nations; 2000. https://www.unscear.org/unscear/en/chernobyl.html
UNSCEAR. Sources and effects of ionizing radiation. UNSCEAR 2008 Report to the General Assembly with Scientific Annexes. Vol. II, Annex D. Health effects due to radiation from the Chernobyl accident. United Nations, New York 2011. https://www.unscear.org/unscear/en/publications/2008_2.html
UNSCEAR. Sources, effects and risks of ionizing radiation. UNSCEAR 2013 Report to the General Assembly with Scientific Annexes. Volume I, Scientific Annex A. United Nations, New York; 2014. https://www.unscear.org/unscear/en/publications/2013_1.html
UNSCEAR. Evaluation of data on thyroid cancer in regions affected by the Chernobyl accident. A white paper to guide the Scientific Committee’s future programme of work. United Nations: New York; 2018. https://www.unscear.org/unscear/en/publications/Chernobyl_WP2017.html
UNSCEAR. Sources, effects and risks of ionizing radiation. UNSCEAR 2020-2021 Report to the General Assembly with Scientific Annexes. Volume II, Scientific Annex B. Levels and effects of radiation exposure due to the accident at the Fukushima Daiichi nuclear power station: implications of information published since the UNSCEAR 2013 Report. United Nations, New York; 2022.
Wakeford R, Auvinen A, Gent RN, Jacob P, Kesminiene A, Laurier D, Schüz J, Shore R, Walsh L, Zhang W.
Re: Thyroid Cancer Among Young People in Fukushima. Epidemiology. 2016; 27(3): e20-1.
Watanobe H, et al. The thyroid status of children and adolescents in Fukushima Prefecture examined during 20–30 months after the Fukushima nuclear power plant disaster: a cross-sectional, observational study. PLoS One. 2015;9:e113804. Erratum.In:PLoSOne.2015;10(7):e0133 345.
Wertelecki W. Chornobyl radiation-congenital anomalies: A persisting dilemma. Congenit Anom (Kyoto). 2021; 61(1):9-13.
WHO. A framework for mental health and psychosocial support in radiological and nuclear emergencies. World Health Organization; 2020. https://www.who.int/publications/i/item/9789240015456
Worgul BV, et al. Cataracts among Chernobyl clean-up workers: implications regarding permissible eye exposures. Radiat Res. 2007; 167: 233-43.
Yeager M, et al. Lack of transgenerational effects of ionizing radiation exposure from the Chernobyl accident. Science. 2021; 372(6543): 725–729.
Yasui S. A recommended epidemiological study design for examining the adverse health effects among emergency workers who experienced the TEPCO Fukushima Daiichi NPP accident in 2011. J Occup Environ Hyg. 2016; 13(5): D77-88.
Zabirova A, Saiko A, Orita M, Furuya F, Yamashita S, Takamura N. Thyroid ultrasound findings in young and middle-aged adults living in the region of the Chornobyl Nuclear Power Plant. Radiat Environ Biophys. 2024; 63(3): 465-468.
Zablotska LB, et al. Radiation and the risk of chronic lymphocytic and other leukemias among Chernobyl cleanup workers. Environ Health Perspect. 2013; 121: 59-65.
Zatsepin I, et al. Down syndrome time-clustering in January 1987 in Belarus: link with the Chernobyl accident? Reprod Toxicol. 2007; 24(3-4): 289-95.
Consulter la note d'information :